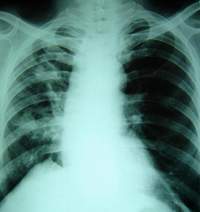
1. Đại cương
Hiện nay có nhiều phương pháp chẩn đoán lao phổi nhưng chẩn đoán quyết định bệnh lao vẫn phải dựa vào những bằng chứng xác định sự có mặt của trực khuẩn lao (BK) ở nơi tổn thương, bằng các kỹ thuật nuôi cấy hoặc mô bệnh. Không có triệu chứng lâm sàng và X-quang đặc thù cho lao phổi, vì nhiều bệnh khác cũng có những triệu chứng như vậy. Tìm thấy tổ chức hoại tử bã đậu ở giải phẫu bệnh lý tổn thương, cũng chưa thể khẳng định là lao, vì nó còn gặp trong các bệnh u hạt (Sacoidose, gôm giang mai, nấm, bụi phổi Beryl, Mycobacteria không điển hình…). Năm 1979 Arif L.A. và cộng sự nghiên cứu thấy những người có HLA – DR2 , HLA-BW15 thì tỷ lệ mắc lao gấp 8 lần người không có các HLA trên. Vì vậy, các phương pháp chẩn đoán được chia làm hai nhóm:
– Các phương pháp chỉ có giá trị định hướng chẩn đoán lao: lâm sàng, X-quang, xét nghiệm miễn dịch, mô bệnh học, công thức máu, dịch màng phổi v.v.
– Các phương pháp chẩn đoán xác định: xét nghiệm nuôi cấy, sinh học phân tử.
https://www.youtube.com/watch?v=qHwchHIF9nM
2. Các phương pháp chẩn đoán có giá trị định hướng lao phổi
2.1. Lâm sàng
– Tiền sử: Cần tìm hiểu các yếu tố nguy cơ của lao phổi như:
+ Tiếp xúc trực tiếp với nguồn lây (bệnh nhân lao phổi có AFB dương tính trong đờm) .
+ Tình trạng suy giảm miễn dịch của cơ thể: mắc các bệnh như đái tháo đường, dùng Corticoid kéo dài, nhiễm HIV/AIDS, tiền sử chấn thương ngực, nghiện rượu, tiêm chích ma tuý, mổ cắt đoạn dạ dày, viêm đại tràng mạn…
+ Tình trạng kinh tế xã hội thấp: nghèo; làm việc nặng, nhọc; suy dinh dưỡng .v.v .
– Triệu chứng lâm sàng
+ Khởi phát bệnh: lao phổi thường khởi phát từ từ, có trường hợp không có triệu chứng lâm sàng. Khởi phát cấp tính thường gặp ở người trẻ hoặc ở các thể lao phổi cấp (lao tản mạn cấp tính, thùy viêm lao, lao phổi bã đậu .v.v.) .
+ Triệu chứng toàn thân: thường có hội chứng nhiễm trùng, nhiễm độc mạn tính như sốt nhẹ kéo dài, thường về chiều, ra mồ hôi đêm, mệt mỏi, ăn kém, mất ngủ, sút cân.
+ Ho: thường ho khan, ho kéo dài gặp phổ biến nhất (trên 3 tuần mà điều trị kháng sinh không kết quả). Có thể ho đờm màu xanh, màu vàng hoặc như chất bã đậu.
+ Ho ra máu: gặp khoảng 30% bệnh nhân, thường gặp ở bệnh nhân có phá hủy hang trên phim X-quang. Mức độ ho ra máu có thể từ nhẹ đến nặng, máu tươi hoặc máu cục, thường có đuôi ho máu .
+ Đau ngực: đau âm ỉ, hay gặp ở vùng đỉnh phổi .
+ Khó thở: hay gặp khi tổn thương phổi rộng, lao phổi tản mạn hoặc có tràn dịch màng phổi kết hợp .
– Trong lao phổi tổn thương thường khu trú vùng đỉnh phổi (92%), do đó các dấu hiệu khám được ở vùng đỉnh phổi có giá trị gợi ý chẩn đoán bệnh. Có thể gặp hội chứng đông đặc điển hình hoặc không điển hình, hay hôị chứng hang. Nhưng các triệu chứng thực thể thường nghèo nàn, đối lập với tổn thương trên X-quang phong phú. Có thể khám phổi không có triệu chứng thực thể gì, chiếm 12-30% các trường hợp lao phổi.
2.2. X-quang
– Những kỹ thuật Xquang thường áp dụng trong chẩn đoán lao phổi:
+ Chiếu X-quang: lợi ích của chiếu X-quang là quan sát hình ảnh động của phổi, thực hiện nhanh, rẻ tiền nên kiểm tra được hàng loạt đối tượng trong thời gian ngắn. Nhược điểm: dễ bỏ sót các tổn thương nhỏ như lao huỵêt, lao kê và lao thâm nhiễm diện hẹp. Hiện nay ít sử dụng.
+ Chụp X-quang chuẩn: Thường chụp X-quang phổi thẳng, nghiêng. Chụp tư thế ưỡn 30o (Tư thế Lordotic): nhằm phát hiện những tổn thương bị xương đòn che lấp.
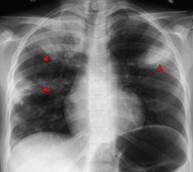
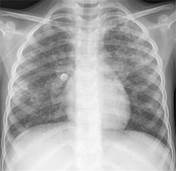
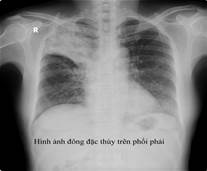
X-quang: Lao thâm nhiễm (mũi tên đỏ hình trái), Hình ảnh đông đặc thùy trên phổi phải (hình giữa), lao kê tản mạn hai phổi (hình phải).
+ Chụp cắt lớp vi tính (Computed Tomography Scanner – CTscan): kĩ thuật này cho phép xác định chính xác vị trí, diện tổn thương và đánh giá chi tiết tổn thương (tổn thương viêm, xơ, vôi, hang, lan tràn .v.v.), nhưng đắt tiền. Do vậy chỉ chỉ định chụp cắt lớp vi tính trong các trường hợp X-quang chuẩn không thấy hoặc nghi ngờ tổn thương.

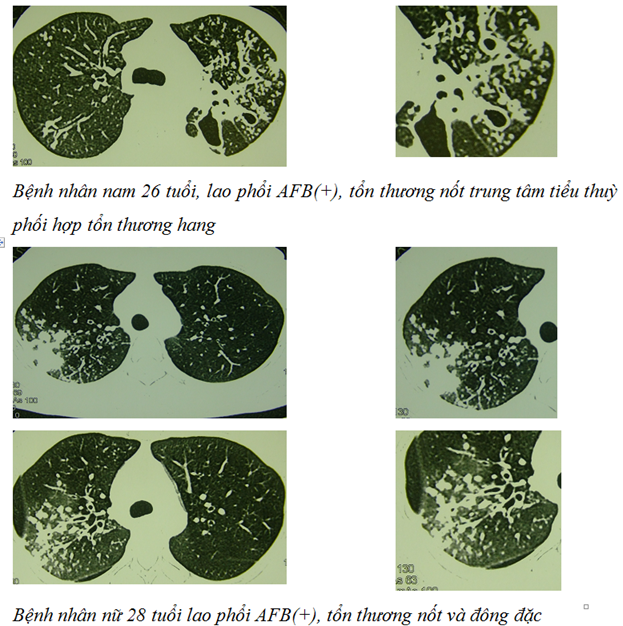
– Đặc điểm tổn thương trên X-quang gợi ý lao phổi:
+ Vị trí tổn thương: hay gặp tổn thương ở vùng cao của phổi (thùy trên, các phân thùy đỉnh) và các phân thùy ở phía sau (phân thùy 2, 6, 10).
+ Tính chất tổn thương: Tổn thương ở một vùng thường đa dạng: tổn thương thâm nhiễm, hang, xơ, vôi xen kẽ nhau. Hay có phá hủy: tạo hang. Tổn thương có xu hướng tiến triển mạn tính: tổn thương xơ, co kéo các thành phần lân cận (khí-phế quản, rốn phổi, rãnh liên thùy, vòm hoành, tim và trung thất .v.v.). Tổn thương ở nhiều nơi: thể hiện tính chất lan tràn. Lan tràn đường máu và bạch huyết (tổn thương đối xứng 2 phổi), lan tràn theo đường phế quản hoặc tiếp cận (tổn thương không đối xứng). Tổn thương thay đổi chậm sau điều trị đặc hiệu (đọc và phân tích phim theo chuỗi): Tổn thương thường thay đổi sau 1 tháng điều trị và sự thay đổi từ từ. Đặc điểm này rất quan trọng trong việc định hướng phân biệt chẩn đoán giữa viêm phổi và lao phổi.
+ Các dạng tổn thương:
. Tốn thương nốt: hạt kê (đường kính < 2mm), nốt nhỏ (2-5 mm), nốt lớn (5- <10 mm).
. Tốn thương thâm nhiễm: các nôt qui tụ thành đám từ 10 mm trở nên, có thể chiếm cả thuỳ hoặc nhiều thuỳ phổi.
. Tổn thương hang: hang nhỏ (đường kính < 2 cm), hang lớn (≥ 4 cm), hang khổng lồ (≥ 6 cm) trong lao phổi thường gặp tổn thương hang. Tổn thương xơ: trong tổn thương lao thường có xơ hoá. Cần tìm dấu hiệu co kéo rốn phổi, co kéo rãnh liên thuỳ bé, cơ hoành, khí quản các khoảng gian sườn hoặc dày dính màng phổi. Là những dấu hiệu nói lên tiến triển mạn tính của bệnh.
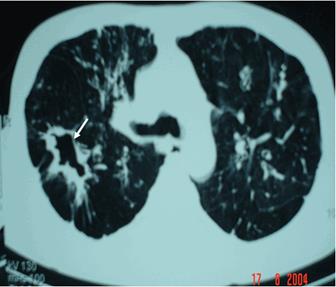
CTscan: Hang lao phổi phải, thành dày, bờ nham nhở.
. Vôi hoá: gặp trong các lao cũ và mạn tính, hoặc di chứng lao ổn định.
Các tổn thương trên có thể phối hợp với nhau và thường khu trú ở đỉnh phổi hoặc các phân thuỳ đỉnh của thuỳ dưới (phân thuỳ VI), với đặc điểm lan tràn theo 3 đường: đường máu và bạch huyết (từ đỉnh phổi này lan sang đỉnh phổi kia), đường phế quản (lan tràn chéo từ đỉnh phổi bên này sang đáy phổi bên kia), đường tiếp cận (sang các phân thuỳ khác hoặc màng phổi).
2.3. Xét nghiệm AFB (Acid Fast Bacilli)
– Kỹ thuật lấy bệnh phẩm:
Bệnh nhân thức dậy buổi sáng sau khi vệ sinh răng miệng xong thì ho và khạc đờm vào cốc đựng bệnh phẩm. Thường lấy bệnh phẩm ở rìa bãi đờm để soi. Nếu bệnh nhân không ho và khạc đờm, có thể cho uống thuốc long đờm hoặc khí dung nước muối sinh lý và vỗ ngực để bệnh nhân dễ khạc đờm. Những trường hợp không có đờm người ta cho bệnh nhân ho trước một lam kính hoặc ngoáy tăm bông ở họng hoặc soi phế quản rửa hút để lấy bệnh phẩm.
– Kỹ thuật soi trực tiếp (Nhuộm Ziehl-Neelsen)
Kỹ thuật này cho phép phát hiện vi khuẩn kháng cồn và axit (AFB: Acid Fast Bacilli) chưa khẳng định được là vi khuẩn lao. Phải có 5000 vi khuẩn / 1 ml đờm thì kết quả mới dương tính. Chương trình chống lao quốc gia qui định đọc kết quả như sau:
+ Khi không có vi khuẩn / 100-300 vi trường: là âm tính.
+ Có 1-9 vi khuẩn / 300 vi trường: ghi số cụ thể đếm được:
. Nếu có: 10-99 vi khuẩn / 100 vi trường = (+ )
. Nếu có 1-9 vi khuẩn / 1 vi trường = ( ++ )
. Nếu có ≥ 10 vi khuẩn / 1 vi trường = ( +++ ).
Với 6 lần dương tính khi soi kính, thì kết quả giá trị tương đương với một lần nuôi cấy.
– Phương pháp thuần nhất đờm:
Làm loãng đờm bằng NaOH rồi ly tâm lấy cặn để nhuộm Ziehl-Neelsen gọi là phương pháp thuần nhất đờm. Kỹ thuật này làm tăng độ nhậy tìm thấy vi khuẩn hơn phương pháp soi trực tiếp.
2.4. Phản ứng Tuberculin
– Tuberculin là bán kháng nguyên, được chiết xuất từ môi trường nuôi cấy BK. Nó gồm nhiều thành phần của BK, cho nên có thể gây phản ứng ở một cơ thể đã nhiễm lao sau tiêm BCG vaccin 48-72h:
– Nếu cục sẩn tại chỗ tiêm có đường kính (d) ≥ 10 mm là dương tính, 5-9 = (±) nghi ngờ, dưới 5 mm là âm tính.
– Mức độ dương tính qui định như sau:
d = 10-14 mm là dương tính nhẹ
d = 15-20 mm là dương tính vừa.
d = 21-30 mm là dương tính mạnh.
Trên 30 mm là dương tính rất mạnh.
Ở trẻ em đã tiêm BCG văcxin thì phản ứng Mantoux phải dương tính từ 12 mm trở lên thì mới coi là dương tính.
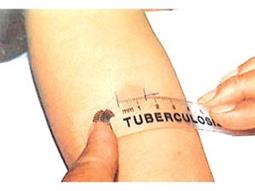
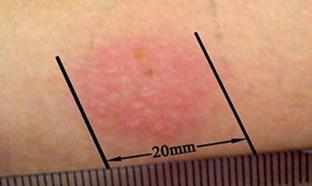
Phản ứng Tuberculin.
– Ý nghĩa của phản ứng :
+ Dương tính: Thể hiện cơ thể đang có kháng thể kháng lao, sức đề kháng và tình trạng miễn dịch đang tốt. Cơ thể đã từng bị nhiễm lao hoặc đã được tiêm BCG vaccin. Trẻ em < 2 tuổi: nếu phản ứng mới chuyển sang dương tính, có giá trị chẩn đoán lao sơ nhiễm.
. Dương tính mạnh gặp trong lao hạch, lao tản mạn bán cấp và mạn tính.
. Người nhiễm Mycobacteria không điển hình phản ứng có thể dương tính yếu.
+ Âm tính: khi chưa từng bị nhiễm lao, suy giảm miễn dịch, nhiễm HIV/AIDS, ung thư, dùng corticoid kéo dài hoặc bệnh lao quá nặng, nhiễm trùng nặng.
2.5. Xét nghiệm máu và dịch màng phổi
2.5.1. Xét nghiệm công thức máu, máu lắng
– Chỉ có giá trị định hướng chẩn đoán lao khi kết hợp với lâm sàng và các xét nghiệm khác .
– Đặc điểm công thức máu, máu lắng: số lượng bạch cầu bình thường hoặc tăng (thường tăng nhẹ), bạch cầu lymphô tăng. Tốc độ lắng máu thường tăng cao.
2.5.2. Xét nghiệm sinh hóa và tế bào dịch màng phổi
– Chỉ có giá trị định hướng chẩn đoán lao màng phổi khi kết hợp với lâm sàng và các xét nghiệm khác .
– Đặc điểm sinh hóa và tế bào dịch màng phổi: dịch tiết (Protein>30g/lít), glucose giảm (thấp hơn glucose huyết thanh cùng thời điểm), tỷ lệ lymphô tăng (thường trên 70% có giá trị định hướng chẩn đoán).
2.5.3. Xét nghiệm nồng độ Interferon g ( INF g)
Interferon-g được tiết ra bởi tế bào lympho T được hoạt hóa khi tiếp xúc với trực khuẩn lao. INF g tăng cả trong máu và dịch màng phổi của bệnh nhân lao .
Định lượng nồng độ INF g thường sử dụng phương pháp miễn dịch huỳnh quang (Immunofluorescence assays) .
Giá trị: Định lượng nồng độ INF g trong huyết thanh hoặc dịch màng phổi có giá trị chẩn đoán lao màng phổi: ở ngưỡng 149pg/ml có độ nhạy khoảng 85%, độ đặc hiệu 97%.
2.5.4. Xét nghiệm ADA (Adenosine deaminase – ADA)
Men ADA được sản xuất từ nhiều tế bào nhưng chủ yếu từ tế bào lympho T hoạt hóa .
Trong tràn dịch màng phổi do lao ADA tăng cả trong máu và dịch màng phổi. Giá trị của xét nghiệm nồng độ ADA trong chẩn đoán tràn dịch màng phổi do lao: Ngưỡng chẩn đoán từ 40-60 u/l. Độ nhạy 91-100%, độ đặc hiệu 81-94%, giá trị dự báo dương tính 84-93%, giá trị dự báo âm tính là 89-100% .
2.6. Các kỹ thuật miễn dịch
2.6.1. Các kỹ thuật phát hiện kháng nguyên của trực khuẩn lao
– Các kháng nguyên bản chất protein:
Các kháng nguyên protein đặc hiệu của M. tuberculosis thường được sử dụng để chẩn đoán bao gồm:
+ Kháng nguyên 38 kDa (còn có tên khác là kháng nguyên 5) là một protein đặc hiệu của phức hệ Mycobacterria tuberculosis. Thường sử dụng kỹ thuật ELISA để phát hiện kháng nguyên này. Độ nhạy của phương pháp đạt tới 67% đối với dịch rửa phế nang và 70-100% với dịch não tuỷ, nhưng độ đặc hiệu chỉ đạt 73% .
+ Phức bộ kháng nguyên 45/47 kDa (APA): được sinh ra trong quá trình phát triển của M. tuberculosis. Thường sử dụng các kháng thể đa dòng của thỏ kháng APA để phát hiện APA. Kỹ thuật này có độ đặc hiệu cao (96%), nhưng độ nhạy lại rất thấp (< 40%) .
– Các kháng nguyên bản chất là glycolipid và lipopolysarcaride:
Đặc trưng là kháng nguyên Lipoarabinomannan (LAM). LAM là một lopopolysarcaride có phân tử lượng 30 đến 40 kDa và là thành phần cấu tạo chủ yếu của vỏ tế bào đặc hiệu cho vi khuẩn lao. Kháng nguyên LAM thường gặp trong đờm, dịch não tuỷ và huyết thanh của bệnh nhân lao. Thường sử dụng các kỹ thuật miễn dịch ngưng kết hồng cầu cừu hoặc kỹ thuật ELISA để phát hiện kháng nguyên này. Đối với lao màng não, phát hiện LAM trong dịch não tuỷ đạt độ nhạy là 88%; Đối với lao phổi kĩ thuật này có độ nhạy đạt từ 71-91%, nhưng độ đặc hiệu lại cao (100%) .
2.6.2. Các xét nghiệm xác định kháng thể kháng lao
Vai trò: ứng dụng để xác định tình trạng nhiễm lao và hỗ trợ chẩn đoán trong trường hợp lao phổi AFB (-) và lao ngoài phổi .
Các kĩ thuật xác định kháng thể kháng lao gồm:
– Kỹ thuật miễn dịch gắn men (Enzzyme liked immuno sorbent assay-ELISA):
Các kháng nguyên được sử dụng trong kĩ thuật ELISA gồm kháng nguyên siêu nghiền, bán tinh chế và tinh chế (LAM, A60, kháng nguyên 5, 16 kDa, DAT, LDS, PGL- TB1,và ES- 31..). Hiệu quả ELISA trong chẩn đoán lao có Se 92,8% và Sp 96% .
– Một số kỹ thuật khác như PCR, HPLC, Accuprobe hybridisation
Các kỹ thuật này cũng đã được ứng dụng để phát hiện kháng thể kháng lao: ưu điểm là rút ngắn được thời gian phát hiện, nhưng đắt tiền và phức tạp, đòi hỏi labo phải được trang bị hiện đại .
2.7. Phương pháp điều trị thử
Phương pháp điều trị thử được áp dụng trong trường hợp chẩn đoán lao phổi AFB (-). Chẩn đoán lao phổi AFB đờm âm tính khi: lâm sàng, Xquang định hướng, AFB (-); hội chẩn chuyên khoa định hướng lao.
Tiến hành điều trị thử kháng sinh chống lao, theo dõi sau 1-3 tháng thấy các triệu chứng lâm sàng và X-quang đáp ứng tốt thì có thể chẩn đoán xác định lao phổi .
3. Các phương pháp có giá trị quyết định chẩn đoán lao phổi
3.1. Nuôi cấy bệnh phẩm
Đây là kĩ thuật xác định chắc nhắn vi khuẩn lao (Bacilli de Koch-BK). Ưu điểm: phân lập, định danh được BK và làm kháng sinh đồ với các thuốc chống lao. Nhược điểm: thời gian có kết quả lâu, đắt tiền, đòi hỏi trang bị phức tạp hơn.
Bệnh phẩm có thể là đờm, dịch tiết phế quản (lấy khi soi phế quản), mẫu mô sinh thiết. Môi trường phải giàu chất khoáng, chất đạm và Vitamin thì BK mới phát triển. Các môi trường đặc: Lowenstein Jensen, Ogawa, Dubos, Middlebrook, gần đây có các môi trường lỏng cho kết quả nhanh hơn.
– Nuôi cấy trong môi trường đặc:
+ Môi trường Lowenstein Jensen ( L. J ) là môi trường đặc gồm có khoai tây, lòng đỏ trứng gà, Glycerin, Asparagin… BK mọc chậm sau 3-6 tuần. Các Mycobacteria không điển hình mọc nhanh trong một tuần. Sau 2 tháng không mọc vi khuẩn thì kết luận là âm tính. Để xác định BK, người ta làm các test Nicain và test khử Nitrat.
+ Các môi trường hiện nay ít được ứng dụng là: Ogawa, Dubos, Middlebrook…
– Nuôi cấy trong môi trường lỏng:
Môi trường chỉ mới được ứng dụng gần đây. Ưu điểm là thời gian mọc của BK nhanh hơn (trung bình 10-14 ngày), nhưng đắt và đòi hỏi trang bị phức tạp hơn. Các môi trường bao gồm:
+ Hệ thống nuôi cấy BACTEC TB 460: được áp dụng từ năm 1980, là môi trường nuôi cấy bán tự động. Nguyên lý: xác định chuyển hóa của BK bằng cách đo nồng độ CO2 giải phóng ra khi phát triển ở môi trường có gắn C14. Thời gian mọc của BK trung bình 8-14 ngày .
+ Hệ thống nuôi cấy MGIT (Multi Growth Indicator Tube-MGIT): nguyên lý kĩ thuật tương tự như hệ thống BACTEC, nhưng thay thế gắn C14 bằng kĩ thuật phát quang (Fluorescene) dưới ánh sáng UV. Kết quả dương tính thì có khoảng 105-106 cfu BK/ml.
3.2. Tiêm truyền trên động vật
Chỉ áp dụng trong phòng thí nghiệm để nghiên cứu, vì tốn kém, có thể phát hiện nhanh sau 9-12 ngày. Dựa vào đo lượng CO2 được đánh dấu đồng vị phóng xạ 14C, do BK hoặc Mycobacteri giải phóng ra trong khi sinh sản. Phương pháp này không phân biệt được là BK hay là Mycobacteria không điển hình.
3.3. Mô bệnh học
Bệnh phẩm là mẫu mô sinh thiết vùng tổn thương, có thể sinh thiết phế quản, sinh thiết xuyên thành phế quản hoặc sinh thiết qua thành ngực.
Hình ảnh điển hình là nang lao: Trung tâm là tổ chức bã đậu, xung quanh là các tế bào bán liên và tế bào khổng lồ Langhans, bên ngoài là các tế bào lympho.
Hình ảnh mô bệnh học điển hình cũng không đặc hiệu cho lao vì còn gặp trong các bệnh u hạt (Sacoidose, gôm giang mai, nấm, bụi phổi Beryl, Mycobacteria không điển hình…).
Khi chọc hút được chất dịch ở nơi tổn thương làm xét nghiệm tế bào học. Phương pháp này chỉ có giá trị gợi ý chẩn đoán phân biệt vì nó chỉ xác định sự có mặt các thành phần của nang lao riêng rẽ, nên có thể dương tính giả hoặc âm tính giả. Đây là kỹ thuật đơn giản ít tai biến.
3.4. Kỹ thuật sinh học phân tử
Một trong những bước tiến vĩ đại của sinh học phân tử trong y học những năm gần đây là kỹ thuật khuếch đại acid nucleic (AND và ARN) trong chẩn đoán lao. Các kỹ thuật sinh học phân tử chẩn đoán lao bao gồm:
– Phản ứng chuỗi polymerase (Polymerase Chain Reaction-PCR):
Nguyên lý kĩ thuật: là kỹ thuật khuyếch đại ADN bằng cách tạo ra hàng triệu bản sao từ 1 chuỗi đích của acid nucleic. ADN polymerase là enzym sao chép ADN, nó có thể tái sao chép nhiều lần đoạn ADN nếu được kích thích đặc hiệu. Xác định sự có mặt của BK thông qua sự khuếch đại đoạn gen ADN đặc hiệu (đoạn IS6110) .
Ưu điểm: độ nhạy và độ đặc hiệu rất cao (chỉ cần một vài BK trong bệnh phẩm kĩ thuật có thể dương tính), kết quả nhanh (24-48 giờ), chẩn đoán kháng thuốc nhanh, có thể tiến hành trên nhiều loại bệnh phẩm khác nhau (đờm, dịch phế quản, dịch màng phổi, dịch não tuỷ .v.v.).
Nhược điểm: giá thành đắt, đòi hỏi trang bị tốn kém; không phân biệt được BK sống hay chết. Dễ có dương tính sai khi bị nhiễm lại sản phẩm PCR (contamination) nếu không tuân thủ chặt chẽ qui trình kỹ thuật vì kỹ thuật có độ nhạy cao, có thể cho âm tính giả do bệnh phẩm chứa nhiều chất ức chế phản ứng hoặc vi khuẩn lao (tỷ lệ khoảng vài phần trăm) không có đoạn IS 6110 trong phân tử ADN. Do vậy kết quả cần phải đối chiếu kết quả PCR với lâm sàng và Xquang trong chẩn đoán lao. Hiện nay thường sử dụng bộ kít PCR đa mồi (…) để tăng hiệu quả chẩn đoán của xét nghiệm PCR.
– Phương pháp khuếch đại trực tiếp (Amplified direct test):
Sử dụng mẫu dò đặc hiệu (probe) để phát hiện những đoạn ARN ribosom (chứ không phải đoạn IS6110 của ADN): dùng những chủng hay phức hợp M. tuberculosis trong môi trường nuôi cấy để phát hiện nhanh vi khuẩn lao .
– Phương pháp AMPLICOR:
Cũng dựa trên nguyên lý chung của kỹ thuật PCR nhưng dùng để khuyếch đại các axit nucleic khác của vi khuẩn lao .
– Kỹ thuật xác định các đoạn axit nucleic hoặc gen đặc trưng cho mỗi chủng BK (Restriction Fragment Length Polymorphism – RFLP):
Có giá trị trong điều tra dịch tễ học bệnh lao, xác định týp, phân týp của vi khuẩn lao, đánh giá lao tái hoạt động hay nhiễm trùng BK mới, xác định kháng thuốc thông qua việc xác định các gen đột biến kháng thuốc với H, Z, R, E, S và nhóm Quinolon; xác định những trường hợp dương tính giả do nuôi cấy vì nhiễm BK trong phạm vi labô đó .
– Phản ứng chuỗi Ligase (Ligase chain reaction – LCR):
Sử dụng enzym Ligase chịu nhiệt để liên kết và khuyếch đại ADN của vi khuẩn lao phục vụ cho chẩn đoán nhanh, trực tiếp. Nguyên lý tương tự như PCR nhưng thay men Polymerase bằng men Ligase chịu nhiệt .
– Xét nghiệm Xpert/MTB:
Nguyên lý: tương tự như PCR nhưng là Real time PCR sử dụng 3 gen mồi đặc hiệu cho độ đặc hiệu cao trong phát hiện BK .
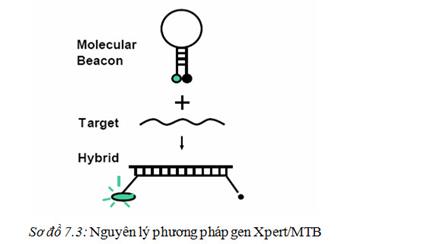
Ưu điểm: độ nhạy và độ đặc hiệu cao (96.7%; 98.6%, giá trị dự báo dương 93.6%, giá trị dự báo âm 99.3%); Kết quả nhanh (trong vòng 2h); xác định nhanh kháng rifampicine (xác định gen rpoB); không phản ứng chéo với các mycobacteria khác.
4. Tiêu chuẩn chẩn đoán lao phổi theo Tổ chức y tế thế giới năm 1998
4.1. Tiêu chuẩn chẩn đoán lao phổi AFB (+)
Chẩn đoán xác định lao phổi AFB (+) khi có 1 trong 3 tiêu chuẩn sau:
– Có tối thiểu một lần xét nghiệm AFB đờm (+) kết hợp với lâm sàng, X-quang định hướng lao.
– Có tối thiểu 2 lần AFB đờm (+) liên tiếp.
– Một tiêu bản đờm AFB (+) và nuôi cấy BK (+).
3.2. Tiêu chuẩn chẩn đoán lao phổi AFB (-)
Chẩn đoán lao phổi AFB âm tính khi có 1 trong 2 tiêu chuẩn sau:
– Xét nghiệm đờm AFB (-) qua 2 lần khám xét cách nhau 2 tuần, mỗi lần xét nghiệm 3 mẫu đờm và có tổn thương nghi lao tiến triển trên X-quang và hội chẩn chuyên khoa định hướng lao .
– Nuôi cấy BK (+).

Để lại một phản hồi